Nowe możliwości w chirurgii filtracyjnej jaskry
– mikroinwazyjna TRABEKULEKTOMIA ab interno – Xen Gel Stent
Trabekulektomia jest najczęściej wykonywanym zabiegiem przeciwjaskrowym. Operacja jest jednak obarczona istotnym ryzykiem wystąpienia powikłań, dlatego opracowano nową technikę wytwarzania dodatkowej drogi odpływu cieczy wodnistej z komory przedniej oka do przestrzeni podspojówkowej.
PROF. DR HAB. N. MED. JACEK P. SZAFLIK 1,2 | LEK. TOMASZ GAŁECKI 2 | LEK. MONIKA ŁAZICKA-GAŁECKA 1,2
1 – KATEDRA I KLINIKA OKULISTYKI II WYDZIAŁU LEKARSKIEGO WARSZAWSKIEGO UNIWERSYTETU MEDYCZNEGO | 2 – SAMODZIELNY PUBLICZNY KLINICZNY SZPITAL OKULISTYCZNY W WARSZAWIE
Jaskra jest jedną z chorób potencjalnie prowadzących do ślepoty. Szacuje się, że na świecie choruje ponad 60 milionów osób. W leczeniu jaskry stosuje się środki farmakologiczne, zabiegi laserowe oraz zabiegi chirurgiczne[1]. Wprowadzona przez Cairnsa w latach 60-tych XX w. trabekulektomia jest najczęściej wykonywanym zabiegiem przeciwjaskrowym. Wykonuje się ją z dostępu ab externo. Po nacięciu spojówki, wytwarzany jest płatek twardówki niepełnej grubości, następnie sklerektomia i irydektomia. Płatek twardówki i spojówka zamykane są przy użyciu szwów. Operacje te obarczone są dużym ryzykiem wystąpienia powikłań, w tym tych zagrażających widzeniu jak: hipotonia, przeciek z pęcherzyka, spłycenie komory przedniej, odłączenie naczyniówki, oraz powikłania związane z pęcherzykiem, jak cystowacenie, włóknienie czy zapalenie[2].
W celu uniknięcia większości z tych powikłań opracowano nową technikę wytwarzania dodatkowej drogi odpływu cieczy wodnistej z oka. Firma AqueSys (obecnie Allergan) opracowała implant XEN, którego technika wszczepiania z dostępu ab interno może wyeliminować większość powikłań, szczególnie wczesnych, charakterystycznych dla trabeculektomii[3].
Implant XEN zbudowany jest z wieprzowej żelatyny, poddanej procesowi cross-linkingu. Jego długość to 6 mm, a światło wewnętrzne to 45 µm. Zasada działania implantu opiera się na prawie Hagena-Poiseuille’a. Zakładając laminarny przepływ przez implant, wykorzystując to prawo można obliczyć opór jaki powinien dawać stent, a także zaprojektować wielkość przepływu przez światło wewnętrzne implantu[4]. Opierając się na wymiarach implantu obliczono, że pozwala on na filtrację o prędkości 2-2,5 ml/min.
Implant oryginalnie dostarczany jest firmowo załadowany do jednorazowego injectora, zakończonego igłą 27G.
Technika operacyjna
Po dezynfekcji skóry przy użyciu powidonu jodyny, dokładnie okleja się pole operacyjne oraz zakłada rozwórkę. Worek spojówkowy dezynfekuje się roztworem powidonu jodyny. Po wypłukaniu jodyny i wysuszeniu spojówki, w kwadrancie górno-nosowym, przy użyciu cyrkla i barwnika zaznacza się punkt oddalony o 3 mm od rąbka. Dwie godziny skroniowo od punktu podaje się 0,1 ml 0,01% MMC podspojówkowo przy użyciu igły 30G. Następnie tępym narzędziem, jak hak zezowy lub gąbką celulozową przesuwa się płyn w kierunku nosowym, w okolicę miejsca, gdzie będzie wszczepiany implant. Mitomycyna powinna być podana ok. 10 minut przed wszczepieniem implantu.
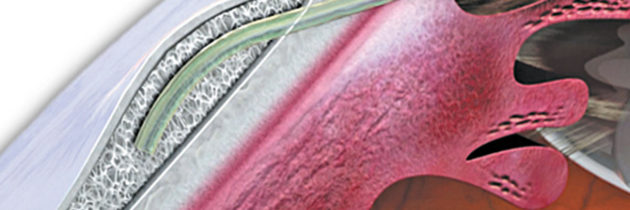
Wykonuje się otwarcie komory przedniej 1,8 mm naprzeciwko miejsca uprzednio oznaczonego miejsca, oraz drugie nacięcie pomocnicze. Komorę przednią wypełnia się wiskoelastykiem kohezyjnym (np. Healon GV). Igłę injectora wprowadza się przez nacięcie i prowadzi w płaszczyźnie tęczówki w poprzek komory przedniej, w kierunku kąta przesączania (ryc. 1.).

Ryc.1 Igła injectora wprowadzona przez nacięcie w rogówce prowadzona w poprzek komory przedniej, w kierunku kąta przesączania
Należy zwrócić szczególną uwagę, aby nie uszkodzić tęczówki i jej nasady. Igłę wprowadza się przez kąt śródtwardówkowo, aż do uwidocznienia jej końcówki pod spojówką. Specjalna konstrukcja igły uniemożliwia jej zbyt głębokie wbicie i perforację spojówki. Igłę następnie odwraca się o 90 stopni w kierunku do centrum. Po ustabilizowaniu injectora wprowadza się implant (ryc. 2., 3.). Jego umiejscowienie w komorze przedniej można zweryfikować stosując soczewkę gonioskopową (ryc. 4.). Po usunięciu wiskoelastyku uszczelnia się nacięcia, co kończy operację. Przy łączonej procedurze z operacją usunięcia zaćmy, można do wszczepienia XENu wykorzystać nacięcia wykorzystywane do fakoemulsyfikacji.

Ryc. 3 Prawidłowo wszczepiony implant, obraz UBM

Ryc. 4 Końcówka XEN widoczna w obrazie gonioskopowym
Technika wszczepienia XENu nie jest czasochłonna, co przy wykonywaniu procedur łączonych z operacją usunięcia zaćmy nie wydłuża w istotny sposób zabiegu.
Leczenie pooperacyjne
Po operacji pacjent standardowo powinien otrzymywać krople steroidowe przez okres minimum około trzech miesięcy. W większości przypadków długość leczenia przeciwzapalnego ustala się indywidualnie. W pierwszym okresie powinien być leczony intensywnie (4-6 razy dziennie), a następnie po dwóch tygodniach dawki powinny być stopniowo redukowane. W przypadku wytworzenia się cysty pęcherzyka filtracyjnego lub włóknienia można wykonać needling, oraz zastosować iniekcje z 5-fluorouracylu.
Wszczepianie implantu XEN wydaje się być bezpieczną i skuteczną procedurą przeciwjaskrową. Jej wyniki prezentujemy na konferencji GlauCat oraz zagranicznych zjazdach, trwają także przygotowania do publikacji. Zastosowanie dostępu ab interno pozwala zaoszczędzić spojówkę dla ewentualnych dalszych procedur. Jest to nowa technika i jej pełna ocena wymaga wykonania dalszych badań i dłuższych obserwacji.
Piśmiennictwo:
1. Tham Y.-C., Li X., Wong T. Y., Quigley H. A., Aung T., Cheng C.-Y. Global prevalence of glaucoma and projections of glaucoma burden through 2040: a systematic review and meta-analysis. Ophthalmology. 2014;121(7):2081–2090. doi: 10.1016/j.ophtha.2014.05.013. [PubMed] [Cross Ref]
2. Gedde S. J., Herndon L. W., Brandt J. D., Budenz D. L., Feuer W. J., Schiffman J. C. Postoperative complications in the tube versus trabeculectomy (TVT) study during five years of follow-up. American Journal of Ophthalmology. 2012;153(5):804–814. doi: 10.1016/j.ajo.2011.10.024. [PMC free article] [PubMed] [Cross Ref]
3. Lewis R. A. Abinterno approach to the subconjunctival space using a collagen glaucoma stent. Journal of Cataract and Refractive Surgery. 2014;40(8):1301–1306. doi: 10.1016/j.jcrs.2014.01.032. [PubMed] [Cross Ref]
4. Sheybani A., Reitsamer H., Ahmed I. Fluid dynamics of a novel micro-fistula implant for the surgical treatment of glaucoma. Investigative Ophthalmology & Visual Science. 2015;56(8):4789–4795. doi: 10.1167/iovs.15-16625. [PubMed] [Cross Ref]


 Instytut Nagrody Zaufania Złoty OTIS
Instytut Nagrody Zaufania Złoty OTIS