Przeszczep warstwowy rogówki
W ostatniej dekadzie obserwuje się światową tendencję wzrostu odsetka przeszczepów warstwowych. Jest to związane z udoskonaleniem techniki zabiegów, a co za tym idzie poprawą pooperacyjnej jakości widzenia. Potwierdzają to dane z piśmiennictwa i nasze własne doświadczenia.
Pośród wszystkich przeszczepów wykonanych w Stanach Zjednoczonych w 2005 roku przeszczepy drążące stanowiły 94 proc., a przeszczepy warstwowe 6 proc. Natomiast w 2013 roku proporcje uległy zmianie. Wykonano wówczas 55 proc. przeszczepów warstwowych i 45 proc. przeszczepów drążących(1). Keenan i wsp. na podstawie analizy przeszczepów wykonanych u pacjentów ze stożkiem rogówki w Wielkiej Brytanii potwierdzają te obserwacje. Odsetek pacjentów, u których wykonano przeszczep drążący zmniejszył się z 88,1 proc. w latach 1999-2000 do 57,1 proc. w latach 2008-2009. W tym samym czasie zwiększyła się częstość przeprowadzanych zabiegów przeszczepów warstwowych przednich z 8,8 proc. do 40,1 proc.(2). Podobna sytuacja dotyczy przeszczepów warstwowych tylnych. Według danych EEBA (European Eye Banking Association) w Europie w 2005 roku wykonano 26 tys. przeszczepów drążących i tylko 500 przeszczepów warstwowych tylnych, a w USA odpowiednio 46 tys. i 1 400. W roku 2014 liczba procedur drążących w Europie spadła do 17 tys., a tylnych wzrosła do 2 tys., zaś w USA do 30 tys., a zabiegów keratoplastyki tylnej aż do 20 tys./rok(3).
Zbliżone tendencje obserwuje się w Polsce. W Samodzielnym Publicznym Klinicznym Szpitalu Okulistycznym w Warszawie w 2000 roku przeszczepy drążące stanowiły 98 proc., a warstwowe jedynie 2 proc. Natomiast w 2014 roku spośród wszystkich wykonanych przeszczepów 37 proc. były to przeszczepy warstwowe, a 63 proc. drążące. Odsetek przeszczepów przednich wzrósł w tym czasie dwukrotnie, a tylnych rośnie z każdym rokiem(4).
Określenie rodzaju planowanego zabiegu
Decyzję o zakwalifikowaniu pacjenta do rodzaju przeszczepu podejmuje się po przeprowadzeniu dokładnego badania przedmiotowego i wykonaniu badań dodatkowych. Należą do nich badanie ultrasonograficzne (UBM, USG), mikroskopia konfokalna rogówki (Confoscan) i optyczna koherentna tomografia przedniego odcinka (AS‑OCT). Dopiero mając pełny wgląd w dokumentację pacjenta podejmuje się decyzję o zakresie przewidywanego zabiegu operacyjnego, jak również o rodzaju znieczulenia.
Przypadki, w których zmiany chorobowe obejmują wszystkie warstwy rogówki, np. w keratopatii pęcherzowej, bliznach pourazowych, perforacjach, są kwalifikowane do przeszczepu drążącego. Jeżeli uszkodzone są tylko niektóre warstwy rogówki, zakres zabiegu można ograniczyć do wymiany zmienionego chorobowo obszaru. W przypadku dystrofii istoty właściwej lub ektazji rogówki przy prawidłowym śródbłonku, można wykonać zabieg przeszczepienia warstwowego przedniego. Jeżeli natomiast przyczyną, dla której pacjent jest kwalifikowany do przeszczepu jest dystrofia śródbłonkowa Fuchsa przy braku istotnych zmian w istocie właściwej preferowany jest przeszczep warstwowy tylny.
W przypadku współistniejących chorób oczu należy je uwzględnić przy planowaniu zakresu zabiegu. Operację przeszczepienia rogówki można rozszerzyć o usunięcie zaćmy z lub bez wszczepu sztucznej soczewki, wszczep wtórny implantu, usunięcie zrostów przednich i wykonanie plastyki tęczówki czy witrektomię.
Obecnie przeszczepianie rogówki wykonywane jest często w znieczuleniu miejscowym, okołogałkowym z sedacją. Znieczulenie ogólne dotchawicze stosuje się u dzieci i młodzieży, osób niepełnosprawnych, niewspółpracujących, głuchoniemych, a także w przypadku zabiegów złożonych (np. przeszczep drążący z usunięciem zaćmy i fiksacją śródtwardówkową sztucznej soczewki).
Przeszczep warstwowy przedni (Anterior Lamellar Keratoplasty, ALK)
Polega na zastąpieniu przednich i środkowych warstw rogówki biorcy zdrową tkanka dawcy. Pozostawia się głębsze warstwy istoty właściwej, błonę Descemeta i śródbłonek biorcy. Wskazaniem do jego przeprowadzenia są:
• przymglenia /blizny sięgające do 1/3 przedniej części istoty właściwej,
• brzeżne lub lokalne ścieńczenie rogówki, naciek lub zmętnienie jak np. w nawrotowym skrzydliku.
Przeszczep warstwowy głęboki przedni (Deep Anterior Lamellar Keratoplasty, DALK)
Nowsza technika przeszczepu warstwowego przedniego, w której cały, nieprzezierny miąższ rogówki powinien zostać usunięty jak najbliżej błony Descemeta. Zaleca się pozostawienie także warstwy Dua (najgłębiej położonych blaszek kolagenu istoty właściwej) w celu lepszej stabilizacji przeszczepionego płatka rogówki. Wskazania:
1. optyczne w celu poprawy widzenia
• stożek rogówki i inne ektazje
• dystrofie miąższu rogówki,
• blizny w przedniej części miąższu, np. po oparzeniach termicznych/chemicznych rogówki,
• stany związane z podwyższonym ryzykiem odrzucenia przeszczepu pełnej grubości, takie jak: zmiany oczne w atopowym zapaleniu skóry i spojówek czy miejscowa neowaskularyzaja,
2. tektoniczne – w celu odtworzenia odpowiedniej grubości w przypadku cienkiej rogówki,
3. sektorowe, np. w ścieńczeniu brzeżnym czy skrzydliku,
4. terapeutyczne.
Przeszczepy warstwowe przednie stanowią wartościową alternatywę dla przeszczepów drżących, w leczeniu ciężkich zakażeń rogówki nieodpowiadających na terapię zachowawczą. W przypadkach, gdzie nie doszło do perforacji rogówki, wykonanie przeszczepu głębokiego warstwowego przedniego jest porównywane pod względem utrzymania przezierności płatka i nawrotu choroby do przeszczepów drążących(5), niosąc jednocześnie korzyści z zachowania własnej błony Descemeta i śródbłonka pacjenta.
Zalety przeszczepów warstwowych przednich w porównaniu do przeszczepów drążących:
• mniejsze ryzyko wystąpienia śródbłonkowej (najgroźniejszej) postaci choroby przeszczepu, ponieważ śródbłonek, główny cel reakcji odrzucania, nie jest przeszczepiany. Mogą natomiast wystąpić łagodniejsze formy choroby przeszczepu (nabłonkowa lub dotycząca istoty właściwej),
• krótszy okres stabilizacji stanu miejscowego: kilka-kilkanaście tygodni,
• mniejszy lub porównywalny astygmatyzm pooperacyjny,
• mniejsza i krótkotrwała utrata komórek śródbłonka. Bezpośrednio po przeszczepach warstwowych przednich obserwuje się nieznaczny spadek gęstość komórek endotelium, który stabilizuje się w ciągu 6 miesięcy; w przypadku przeszczepów drążących obserwuje się stały spadek gęstości tych komórek. Po 12 miesiącach średni ubytek komórek śródbłonka wynosi 27,7% w przeszczepach drążących i 12,9% w warstwowych przednich(6),
• krótszy czas stosowania steroidów miejscowo –mniejsze ryzyko zaćmy i jaskry wtórnej,
• technika optymalna dla ludzi młodych, ponieważ zaoszczędzony jest zdrowy śródbłonek biorcy,
• w przypadku przeniesienia infekcji bakteryjnej z dawcy do biorcy ogranicza się głównie do zapalenia rogówki, nie rozprzestrzeniając się do wnętrza gałki ocznej, jak to ma miejsce po przeszczepie drążącym.
Wady w porównaniu z keratoplastyką drążącą:
• skomplikowana i czasochłonna technika,
• dłuższa krzywa uczenia,
• mogą powstać przymglenia na powierzchni styku lub fałdy błony Descemeta, które zaburzają widzenie,
• możliwość wystąpienia perforacji (9-23 proc.) i konieczność przeprowadzenia keratoplastyki drążącej.
Przeszczep warstwowy głęboki przedni
Transplantacja płatka dawcy
Płatek rogówkowo-twardówkowy układa się na specjalnej płytce trepanu ręcznego śródbłonkiem ku górze (Ryc. 1.). Następnie okrągłym ostrzem wycina się fragment rogówki o pożądanej średnicy. Do czasu użycia materiał dawcy przechowywany jest w płynie konserwującym. Błonę Descemeta i śródbłonek usuwa się mechanicznie przy użyciu chirurgicznej gąbki celulozowej.
Wycięcie (trepanowanie) płatka biorcy w przeszczepie warstwowym głębokim przednim
Trepanowanie rogówki biorcy przeprowadza się z użyciem trepanu próżniowego (Ryc. 2.). Po jego przyssaniu do gałki ocznej obraca się okrągłe ostrze trepanu, do momentu osiągnięcia pożądanej głębokości. Cięcie w rogówce biorcy można również wykonać za pomocą trepanów ręcznych lub elektrycznych, bądź lasera femtosekundowego, po jego zadokowaniu do gałki ocznej.
W przypadku przeszczepu warstwowego głębokiego przedniego po głębokim nacięciu rogówki (około 80 proc. grubości istoty właściwej) usuwa się przednie jej warstwy. Do tego celu można wykorzystać kilka technik. Najstarszą metodą, jednak obarczoną dużym ryzykiem perforacji jest technika manualna, w której chirurg warstwa po warstwie wycina istotę właściwą do pożądanej głębokości. Obecnie, w celu lepszego preparowania włókien miąższu, między głębokie warstwy istoty właściwej, a błonę Descemeta podaje się igłą powietrze, płyn, bądź wiskoelastyk. Do płaszczyznowego cięcia rogówki można również używać mikrokeratomów. Jednak najlepsze efekty daje technika „big-bubble” według Anwara. W tej metodzie wprowadza się igłę w głębokie warstwy istoty właściwej na 3-4 mm od brzegu trepanacji skośnie w dół. Podanie powietrza powoduje kopulaste odłączenie błony Descemeta. W ten sposób istota właściwa jest oddzielona od błony Descemeta i może być usunięta pozostawiając cienką warstwę włókien na pęcherzyku powietrza. Następnie spiczastym ostrzem rozdziela się pęcherzyk i po wprowadzeniu wiskoelastyku wycina się resztkowy miąższ kwadrant po kwadrancie, aż do odsłonięcia lśniącej błony Descemeta. Obecnie technikę „big-bubble” ulepsza się przeprowadzając nacięcia z użyciem lasera femtosekundowego. Pozwala to precyzyjnie uwidocznić miejsce podania powietrza do tylnej części miąższu, a tym samym zmniejszyć ryzyko perforacji błony Descemeta.
Wszycie płatka dawcy w przeszczepie warstwowym głębokim przednim
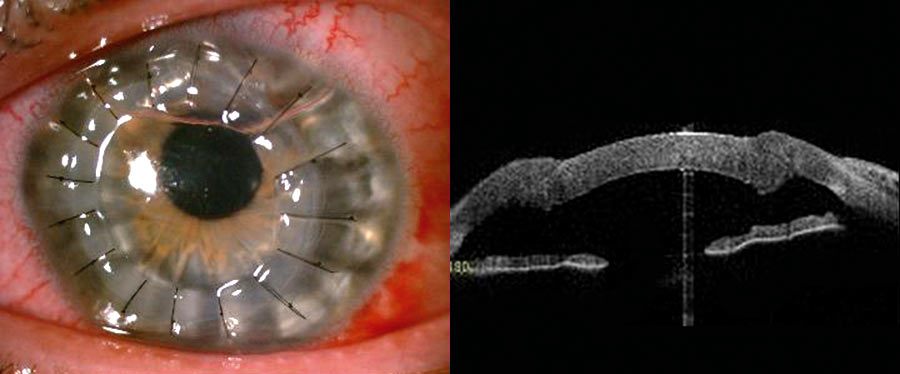
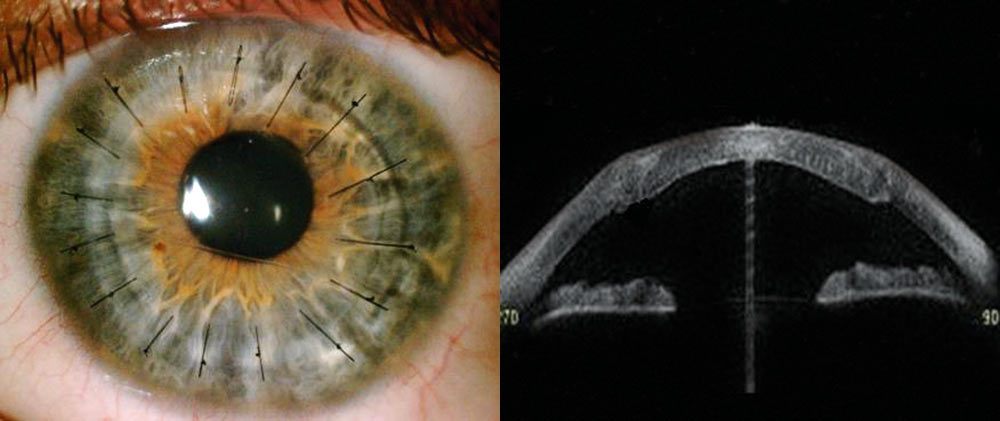
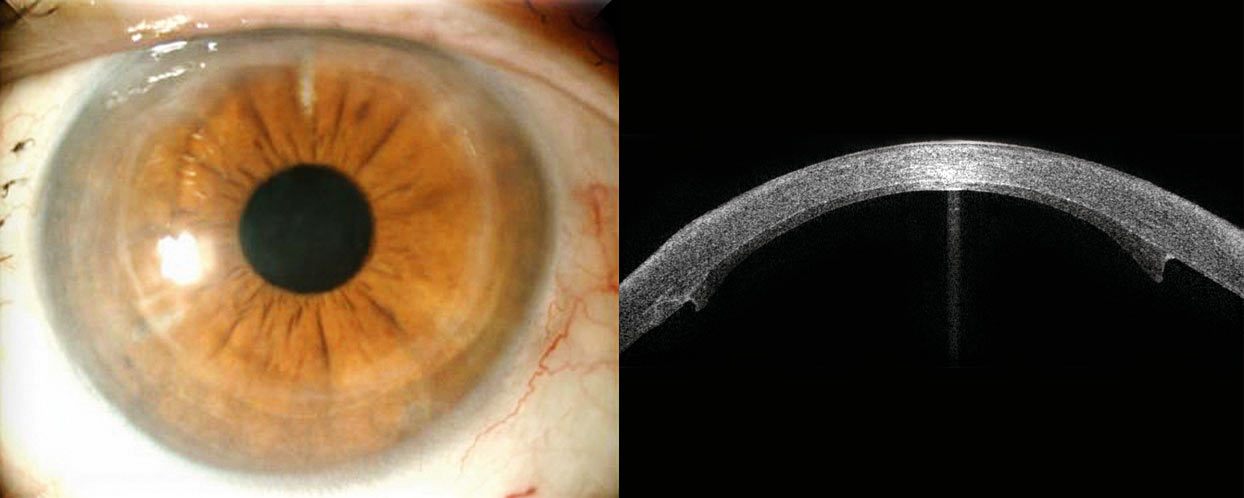
Płatek dawcy początkowo przyszywa się czterema szwami głównymi na godzinie 12, 6, 3 i 9, i w zależności od warunków zakłada się 12-18 szwów pojedynczych (często w przypadku przeszczepu warstwowego przedniego), 8 szwów pojedynczych i szew ciągły lub 2 szwy ciągłe (Ryc. 3.). Supełki szwów pojedynczych przeciąga się w głąb istoty właściwej rogówki, tak aby nie drażniły.
Na zakończenie zabiegu do komory przedniej podaje się pęcherzyk powietrza, okołogałkowo iniekcję z depo-medrolu i podspojówkowo BDL (biodacyna-dexaven-lidokaina).
Przeszczepy warstwowe tylne (Endothelial Keratoplasty, EK)
Keratoplastyka endotelialna została zapoczątkowana przez Gerrita Mellesa w drugiej połowie lat 90. XX wieku(7) i zrewolucjonizowała możliwości terapeutyczne w przypadkach keratopatii pęcherzowej i chorób śródbłonka rogówki, w których jeszcze 15-20 lat temu jedynym postępowaniem chirurgicznym była keratoplastyka drążąca. Przeszczep warstwowy tylny to obecnie „złoty standard” w leczeniu chorób błony Descemeta i śródbłonka rogówki w Europie i USA.
Choroby, w których dochodzi do upośledzenia funkcjonowania komórek śródbłonka i które stanowią wskazania do przeszczepu warstwowego tylnego to:
• dystrofia Fuchsa (FECD) i keratopatia pęcherzowa,
• pierwotna niewydolność komórek śródbłonka (bez FECD),
• dystrofia polimorficzna tylna (PPD),
• zespół śródbłonkowy tęczówkowo-rogówkowy (ICE),
• jatrogenne uszkodzenie śródbłonka (np. powikłanie operacji zaćmy) – keratopatia pęcherzowa w pseudosoczewkowości lub afakii.
W każdym rodzaju obecnie wykonywanej keratoplastyki selektywnej tylnej, u biorcy przeszczepu usuwana jest jedynie błona Descemeta ze zmienionym śródbłonkiem i zastępowana prawidłowymi warstwami rogówki dawcy w zależności od techniki zabiegu – tylko śródbłonkiem na błonie Descemeta lub śródbłonkiem, błoną Descemeta wraz z cienkim fragmentem przylegającego do niej miąższu o grubości 100-200 µm. Materiał do przeszczepu pochodzi od zmarłych dawców.
Rodzaje przeszczepów tylnych rogówki
• PLK (posterior lamellar keratoplasty, G. Melles 1998)(7),
• DLEK (deep lamellar endothelial keratoplasty, M. Terry)(8),
• DSEK (Descemet’s stripping endothelial keratoplasty, M. Gorovoy i F. Price Jr, 2004)(9),
• DSAEK (Descemet’s stripping automated endothelial keratoplasty) z użuciem mikrokeratomu,
• DMEK (Descemet’s membrane endothelial keratoplasty, zespół Mellesa 2008(10), zespół Pricea 2009 (11)),
• DMAEK (Descemet’s Membrane Automated Endothelial Keratoplasty, McCauley i Price 2009) – to rodzaj zabiegu hybrydowego DMEK z DSAEK(12),
• DMEK-S (P. Studeny, 2010) – płatek hybrydowy preparowany manualnie(13),
• UT-DSAEK (Utra-thin Descemet’s stripping automated endothelial keratoplasty, M. Busin 2009) – ultracienki płatek dawcy preparowany przez dwa cięcia mikrokeratomem.(14)
Zalety przeszczepów warstwowych tylnych w porównaniu do przeszczepów drążących:
• znacznie lepsza ostrość wzroku i jakość widzenia,
• mniejsza ingerencja chirurgiczna i mniejsze obciążenie dla pacjenta,
• szybsze gojenie i rehabilitacja wzrokowa,
• dobra przewidywalność – mały odsetek niepowodzeń,
• brak szwów rogówkowych nie powoduje powstania astygmatyzmu, stymulacji wrastania naczyń i ryzyka rozszczelnienia rany,
• mniejsze ryzyko odrzutu, a w razie jego wystąpienia lepsze rokowanie wyleczenia.
Wady w porównaniu z keratoplastyką drążącą:
• dłuższa krzywa uczenia.
DSAEK jest do dziś preferowaną metodą keratoplastyki selektywnej tylnej. Technika zabiegu jest następująca:
Przygotowanie płatka dawcy
Płatek rogówkowo-twardówkowy o średnicy 16-19 mm umieszczany jest na sztucznej komorze przedniej (Moria) śródbłonkiem ku dołowi. Po osiągnięciu ciśnienia około 90 mmHg mierzona jest grubość płatka w centrum przy użyciu pachymetrii ultradźwiękowej. Następnie zostaje odcięta przednia warstwa rogówki mikrokeratomem automatycznym z głowicą 300 lub 350 µm w zależności od wyniku pachymetrii. W niektórych ośrodkach do cięcia używany jest laser femtosekundowy. Pozostała loża składająca się z tylnej części istoty właściwej, błony Descemeta i śródbłonka jest ponownie mierzona pachymetrycznie (pożądana wartość to 100‑120 µm), następnie odciętą wcześniej przednią część rogówki dawcy z powrotem umieszcza się w pierwotnym położeniu, markerem zaznaczane są punkty orientacyjne. Płatek rogówkowo-twardówkowy przenoszony jest ze sztucznej komory na podstawę trepanu ręcznego, precyzyjnie pozycjonowany. Trepanem ręcznym o średnicy 8,0-9,0 mm wycina się płatek rogówkowy, który następnie jest zabezpieczany w niewielkiej ilości płynu konserwującego.
Przebieg operacji u biorcy
Zabieg wykonywany jest najczęściej w znieczuleniu miejscowym: okołogałkowym i NLA. W części skroniowej po odpreparowaniu spojówki gałkowej wykonywany jest tunel twardówkowo-rogówkowy szerokości 4,5-5,0 mm oraz paracentezy na godzinie 12.00 i dodatkowe paracentezy w kwadrantach górnym i dolnym – ich ilość zależy od sposobu wszczepiania płatka dawcy. Niektórzy chirurdzy wykonują otwarcie w przeziernej rogówce, może ono skutkować jednak zwiększeniem astygmatyzmu pooperacyjnego. Komora przednia wypełniana jest wiskoleastykiem. Na powierzchni rogówki znacznikiem określa się obszar o średnicy 8,0-9,0 mm w rzucie którego przy pomocy specjalnego haczyka dokonuje się usunięcia chorej błony Descemeta wraz ze śródbłonkiem biorcy (stripping). W zależności od stopnia zaawansowania keratopatii wykonywana jest lub nie abrazja nabłonka w celu lepszej wizualizacji wewnątrzgałkowych etapów zabiegu. Odłączona błona Descemeta biorcy usuwana jest z komory, a brzeg descemetoreksji adaptuje się szeroką zakrzywiona szpatułką (scrapping). W dolnej partii tęczówki obwodowo na godz. 6.00 wykonywana jest chirurgiczna irydotomia lub poszerza się istniejącą irydotomię laserową. Bardzo istotne jest dokładne wypłukanie wiskoelastyku z komory przedniej, którego pozostałość mogłaby uniemożliwić integrację płatka dawcy z rogówką biorcy. Wszczepienie płatka dawcy można wykonać kilkoma metodami: np. przy pomocy specjalnej pęsety (np. pęsetą Charlie’go skonstruowaną przez Terryego) lub przy użyciu rynienki Busina. Pierwszy sposób jest szybszy, ale wymaga odpowiednio głębokiej komory przedniej. W drugim sposobie do komory przedniej biorcy zakłada się infuzję płynu BSS, płatek dawcy umieszcza w rynience Busina, którą przykłada się do skroniowego tunelu rogówkowo-twardówkowego, a pęsetą Busina wprowadzoną przez przeciwległy port w części nosowej wciąga płatek dawcy dokomorowo. Podanie powietrza pod płatek przypiera go do tkanki biorcy. Po osiągnięciu optymalnego ciśnienia (przejściowo nawet około 30 mmHg), gładząc rogówkę dokonuje się ostatecznego ustawienia płatka i wypycha resztkę płynu lub powietrza z przestrzeni między tkankami dawcy i biorcy. Na tunel zakładane są szwy, a w razie abrazji nabłonka zakładana jest opatrunkowa soczewka kontaktowa. W przypadku współistniejącej zaćmy wykonywana jest procedura potrójna w kolejności: fakoemulsyfikacja zaćmy, wszczepienie implantu do torby tylnej, przeszczep warstwowy tylny.
Bardzo ważny dla osiągnięcia efektu zabiegu jest reżim pooperacyjny: pacjent leży w pozycji płasko na wznak przez kilka godzin. Do potencjalnych powikłań śródoperacyjnych należą: uszkodzenie tkanki dawcy, umieszczenie płatka dawcy złą stroną w stosunku do tkanki biorcy, podanie powietrza między rogówkę biorcy a płatek dawcy, krwawienie z irydotomii, śródoperacyjny blok źreniczny. Do wczesnych powikłań pooperacyjnych należą: dyslokacja płatka oraz blok źreniczny. W przypadku pierwszego powikłania wykonuje się repozycję płatka z podaniem powietrza do komory przedniej, natomiast w przypadku drugiego leczeniem jest farmakologiczna dylatacja źrenicy i obniżanie ciśnienia wewnątrzgałkowego (pacjent musi leżeć na wznak).
Opieka nad pacjentem po keratoplastyce warstwowej, jak w każdym przypadku przeszczepu rogówki, wymaga wielomiesięcznej obserwacji. Leczenie farmakologiczne w początkowym okresie po zabiegu składa się z antybiotyków, leków przeciwzapalnych, steroidów w kroplach, a czasem także doustnych. Po około 4 tygodniach leki redukuje się do kropli steroidowych, które utrzymuje się przez około 2 lata, a w trzecim roku stopniowo zmniejsza dawkowanie, aż do odstawienia leków w przypadkach niepowikłanych. W przypadku przeszczepów warstwowych przednich szwy zdejmuje się zazwyczaj po około 12 miesiącach po zabiegu. Schematy dawkowania i całkowity czas terapii mogą różnić się w zależności od ośrodka i chirurga.
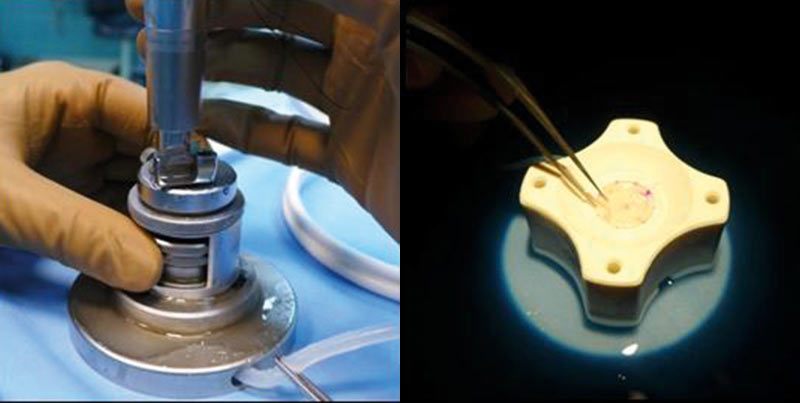
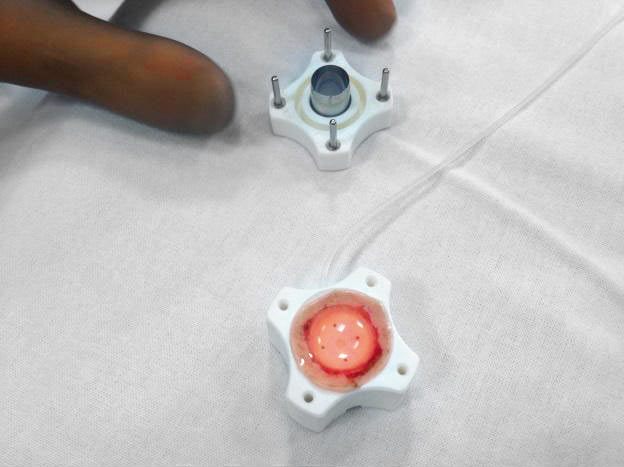
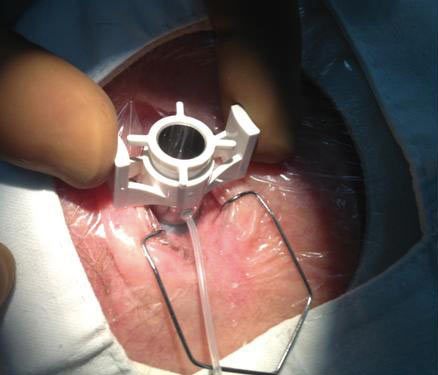
Ryc. 5. Preparowanie płatka do przeszczepu tylnego – wycięcie automatycznym mikrokeratomem i na bloczku trepanem ręcznym
Podsumowanie
Przeszczepy warstwowe wiążą się z mniejszą liczbą śród- i pooperacyjnych powikłań, dają lepsze wyniki refrakcyjne, pozwalają na szybszą rehabilitację widzenia i zmniejszają ryzyko odrzucenia przeszczepu. Analizy szacujące stosunek kosztów interwencji chirurgicznej do korzyści, jakie ona niesie w rozumieniu poprawy wyników klinicznych i jakości życia pacjentów wykazały, że przeszczepy warstwowe są bardziej efektywne ekonomicznie i społecznie w porównaniu z przeszczepami drążącymi(15).
tekst dr n. med. Justyna Izdebska, lek. Monika Udziela, prof. dr hab. med. Jacek P. Szaflik
Katedra i Klinika Okulistyki II WL Warszawskiego Uniwersytetu Medycznego Samodzielny Publiczny Kliniczny Szpital Okulistyczny w Warszawie
Piśmiennictwo:
1. U.S. Eye Banking Statistical Report 2013
2. Keenan T.D., Jones M.N., Rushton S., Carley F.M., National Health Service Blood and Transplant Ocular Tissue Advisory Group and Contributing Ophthalmologists (Ocular Tissue Advisory Group Audit Study 8) Trends in the indications for corneal graft surgery in the United Kingdom: 1999 through 2009. Arch Ophthalmol. 2012 May; 130(5):621-8.
3. Dane EEBA 2014
4. Raport roczny SPKSO Warszawa 2000-2014
5. Reinhart W.J., Musch D.C., Jacobs D.S., et al. Deep anterior lamellar keratoplasty as an alternative to penetrating keratoplasty: a report by the American Academy of Ophthalmology. Ophthalmology 2011; 118:209–18.
6. Cheng Y.Y., Visser N., Schouten J.S., et al. Endothelial cell loss and visual outcome of deep anterior lamellar keratoplasty versus
penetrating keratoplasty: a randomized multicenter clinical trial. Ophthalmology 2011; 118:302–9.
7. Melles G.R., Eggink F.A., Lander F., et al. A surgical technique for posterior lamellar keratoplasty. Cornea. 1998; 17(6):618-626.
8. Terry M.A., Ousley P.J. Deep lamellar endothelial keratoplasty visual acuity, astigmatism, and endothelial survival in a large prospective series. Ophthalmology. 2005; 112:1541-8
9. Gorovoy M., Price F.W. New technique transforms corneal transplantation. Cataract Refract Surg Today.2005; 11:55-8.
10. Melles G.R., Ong T.S., Ververs B., van der Wees J. Preliminary clinical results of Descemet membranę endothelial keratoplasty. Am J Ophthalmol. 2008; 145:222-7
11. Price M.O., Giebiel A.W., Fairchild K.M., Price F.W. Jr. Descemet’s membrana endothelial keratolasty: Prospective multicenter study of visual and refractive outcomes and endothelial survival. Ophthalmology. 2009; 116:2361-8
12. McCauley M.B., Price F.W., Price M.O. Descemet membrane automated endothelial keratoplasty: hybrid technique combining DSAEK stability with DMEK visual results. J Cataract Refract Surg 2009; 35:1659–64.
13. Studeny P., Farkas A., Vokrojova M., et al. Descemet membrane endothelial keratoplasty with a stromal rim (DMEK-S). Br J Ophthalmol 2010; 94:909–14
14. Busin M. Tools and techniques Ultra-thin DSAEK. Online 2012Feb: www.eyeworld.org/printarticle.php?id=6198
15. van den Biggelaar F.J., Cheng Y.Y., Nuijts R.M., et al. Economic evaluation of deep anterior lamellar keratoplasty versus penetrating keratoplasty in the Netherlands. Am J Ophthalmol 2011;151:449–59.

 Instytut Nagrody Zaufania Złoty OTIS
Instytut Nagrody Zaufania Złoty OTIS